Nội dung Ôn tập môn Hóa Học 9 - Chủ đề 1: Ôn tập đầu năm
I-KIẾN THỨC TRỌNG TÂM CẦN NẮM
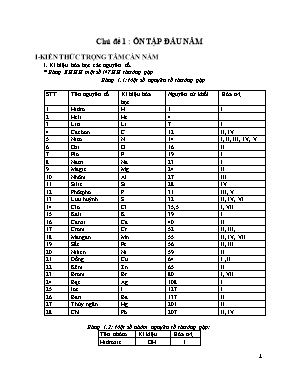
1. Kí hiệu hóa học các nguyên tố.
* Bảng KHHH một số NTHH thường gặp
2. Phân tử khối
Phân tử khối là khối lượng phân tử tính bằng đơn vị cacbon. Phân tử khối bằng tổng nguyên tử khối của các nguyên tử trong phân tử.
3. Lập công thức hóa học (CTHH) của hợp chất khi biết hóa trị
- Viết CT dạng chung: AxBy.
- Áp dụng qui tắc hóa trị: x.a = y.b
- Rút ra tỉ lệ: x/y = b/a = b’/a’ (tối giản)
- Viết CTHH.
4. Các bước lập phương trình hóa học
Bước 1: Viết sơ đồ phản ứng, gồm công thức hóa học của các chất phản ứng và sản phẩm.
Bước 2: Cân bằng số nguyên tử mỗi nguyên tố: Đặt hệ số sao cho số nguyên tử của mỗi nguyên tố ở hai vế bằng nhau. ( lưu ý các phương pháp như làm lẻ thành chẵn, cân bằng theo nhóm nguyên tử,.....)
Bước 3: Viết phương trình hóa học.
5. Các công thức tính toán hóa học cơ bản
- Chuyển đổi giữa khối lượng chất và số mol
Trong đó: m là khối lượng chất
M là khối lượng mol (bằng nguyên tử khối hoặc phân tử khối của chất)
n là số mol chất
-Chuyển đổi giữa thể tích chất khí và số mol
Trong đó: V là thể tích chất khí ở điều kiện tiêu chuẩn
n là số mol chất khí
6. Tính theo phương trình hóa học:
- Các bước giải
- Chuyển dữ kiện bài toán về số mol (bằng các công thức chuyển đổi)
- Viết phương trình hóa học.
- Dựa vào phương trình hóa học để tìm số mol các chất tham gia, sản phẩm.
- Giải quyết yêu cầu bài toán (bằng các công thức chuyển đổi)
b, Các ví dụ minh họa
Tóm tắt nội dung tài liệu: Nội dung Ôn tập môn Hóa Học 9 - Chủ đề 1: Ôn tập đầu năm
Chủ đề 1 : ÔN TẬP ĐẦU NĂM I-KIẾN THỨC TRỌNG TÂM CẦN NẮM 1. Kí hiệu hóa học các nguyên tố. * Bảng KHHH một số NTHH thường gặp Bảng 1.1: Một số nguyên tố thường gặp STT Tên nguyên tố Kí hiệu hóa Nguyên tử khối Hóa trị học 1 Hidro H 1 I 2 Heli He 4 3 Liti Li 7 I 4 Cacbon C 12 II, IV 5 Nitơ N 14 I, II, III, IV, V 6 Oxi O 16 II 7 Flo F 19 I 8 Natri Na 23 I 9 Magie Mg 24 II 10 Nhôm Al 27 III 11 Silic Si 28 IV 12 Phôtpho P 31 III, V 13 Lưu huỳnh S 32 II, IV, VI 14 Clo Cl 35,5 I, VII 15 Kali K 39 I 16 Canxi Ca 40 II 17 Crom Cr 52 II, III, 18 Mangan Mn 55 II, IV, VII 19 Sắt Fe 56 II, III 20 Niken Ni 59 II 21 Đồng Cu 64 I ,II 22 Kẽm Zn 65 II 23 Brom Br 80 I, VII 24 Bạc Ag 108 I 25 Iot I 127 I 26 Bari Ba 137 II 27 Thủy ngân Hg 201 II 28 Chì Pb 207 II, IV Bảng 1.2: Một số nhóm nguyên tố thường gặp: Tên nhóm Kí kiệu Hóa trị Hidroxit OH I 1 Nitrat NO3 I Amoni NH4 I Sunfat SO4 II Cacbonat CO3 II Sunfit SO3 II Photphat PO4 III 2. Phân tử khối Phân tử khối là khối lượng phân tử tính bằng đơn vị cacbon. Phân tử khối bằng tổng nguyên tử khối của các nguyên tử trong phân tử. VD:O2 = 2.16 = 32 đvC ; Cl2 = 2.35,5 = 71 đvC. CaCO3 = 40 + 12 + 16.3 = 100 đvC ; Cu(OH)2 = 64 + ( 16 + 1 ). 2 = 98 đvC. 3. Lập công thức hóa học (CTHH) của hợp chất khi biết hóa trị - Viết CT dạng chung: AxBy. - Áp dụng qui tắc hóa trị: x.a = y.b - Rút ra tỉ lệ: x/y = b/a = b’/a’ (tối giản) - Viết CTHH. VD Lập CTHH cho hợp chất tạo bởi: Al và O Giải: III II CT dạng chung: AlxOy. - Theo qui tắc hóa trị: x×III = y×II x II - Rút ra tỉ lệ: y III => x = 2; y = 3 - CTHH: Al2O3 VD: lập CTHH của hợp chất tạo bởi Cu hóa trị II và nhóm SO4 hóa trị II - Viết CT chung dạng: Cux(SO4)y - Theo quy tắc hóa trị: x×II = y×II - Chuyển thành tỉ lệ: - => x = 1; y = 1 - CTHH của hợp chất CuSO4 4. Các bước lập phương trình hóa học Bước 1: Viết sơ đồ phản ứng, gồm công thức hóa học của các chất phản ứng và sản phẩm. 2 Bước 2: Cân bằng số nguyên tử mỗi nguyên tố: Đặt hệ số sao cho số nguyên tử của mỗi nguyên tố ở hai vế bằng nhau. ( lưu ý các phương pháp như làm lẻ thành chẵn, cân bằng theo nhóm nguyên tử,.....) Bước 3: Viết phương trình hóa học. VD1: Cân bằng PTHH Al + HCl → AlCl3 + H2 - Ta chỉ việc thêm hệ số 2 vào trước AlCl 3 để cho số nguyên tử Cl chẵn. Khi đó, vế phải có 6 nguyên tử Cl trong 2AlCl3, nên vế trái thêm hệ số 6 trước HCl. Al + 6HCl → 2AlCl3 + H2 - Vế phải có 2 nguyên tử Al trong 2AlCl3, vế trái ta thêm hệ số 2 trước Al. 2Al + 6HCl → 2AlCl3 + H2 - Vế trái có 6 nguyên tử H trong 6HCl, nên vế phải ta thêm hệ số 3 trước H2. 2Al + 6HCl → 2AlCl3 + 3 H2 VD2: KClO3 → KCl + O2 - Ta thấy số nguyên tử oxi trong O 2 là số chẵn và trong KClO 3 là số lẻ nên đặt hệ số 2 trước công thức KClO3. 2KClO3 → KCl + O2 - Tiếp theo cân bằng số nguyên tử K và Cl, đặt hệ số 2 trước KCl. 2KClO3 → 2KCl + O2 - Cuối cùng cân bằng số nguyên tử oxi nên đặt hệ số 3 trước O2. 2KClO3 → 2KCl + 3O2 VD3: Al + O2 → Al2O3 - Số nguyên tử oxi trong Al2O3 là số lẻ nên thêm hệ số 2 vào trước nó. Al + O2 → 2Al2O3 Khi đó, số nguyên tử Al trong 2Al2O3 là 4. Ta thêm hệ số 4 vào trước Al. 4 Al + O2 → 2Al2O3 - Cuối cùng cân bằng số nguyên tử oxi, vế phải số nguyên tử oxi trong 2Al 2O3 là 6, vế trái ta thêm hệ số 3 trước O2. 3 4Al + 3O2 → 2Al2O3 5. Các công thức tính toán hóa học cơ bản - Chuyển đổi giữa khối lượng chất và số mol m m n m n.M M M n Trong đó: m là khối lượng chất M là khối lượng mol (bằng nguyên tử khối hoặc phân tử khối của chất) n là số mol chất -Chuyển đổi giữa thể tích chất khí và số mol V n V n.22 ,4 khí 22 ,4 Trong đó: V là thể tích chất khí ở điều kiện tiêu chuẩn n là số mol chất khí 6. Tính theo phương trình hóa học: a. Các bước giải - Chuyển dữ kiện bài toán về số mol (bằng các công thức chuyển đổi) - Viết phương trình hóa học. - Dựa vào phương trình hóa học để tìm số mol các chất tham gia, sản phẩm. - Giải quyết yêu cầu bài toán (bằng các công thức chuyển đổi) b, Các ví dụ minh họa VD1 : Tính khối lượng CaO thu được khi nung hoàn toàn 50 gam CaCO3. Biết PTHH t0 xảy ra như sau: CaCO3 CaO + CO2 - Tính số mol chất đã biết theo đề bài. m 50 n 0,5(mol) CaCO3 M 100 Lập PTHH. t0 CaCO3 CaO + CO2 1mol 1 mol 0,5mol x mol Tính số mol CaO theo PTHH 0,5.1 x 0,5(mol) 1 Tính khối lượng CaO : mCaO n.M 0,5.56 28(g) VD 2: Cho Zn tác dụng với axit clohiđric HCl thu được ZnCl2 và 11,2 lít khí H2 (đktc). a. Lập PTHH xảy ra. b. Tính khối lượng Zn và khối lượng axit clohiđric HCl cần dùng. V 11,2 n 0,5(mol) H2 22,4 22,4 4 Zn + 2HCl ZnCl2 + H2 1mol 2mol 1mol xmol ymol ← 0,5mol 0,5.1 x 0,5(mol) 1 0,5.2 y 1(mol) 1 m n.M 0,5.65 32(g) => Zn mHCl n.M 1.36,5 36,5(g) 7. PHÂN LOẠI CÁC HỢP CHẤT VÔ CƠ oxit Axit bazơ muối Là hợp chất của oxi Là hợp chất mà phân Là hợp chất mà phân tử Là hợp chất mà phân với 1 nguyên tố khác tử gồm 1 hay nhiều gồm 1 nguyên tử kim tử gồm kim loại liên nguyên tử H liên kết loại liên kết với 1 hay kết với gốc axit. với gốc axit nhiều nhóm OH Gọi nguyên tố trong Gọi gốc axit là B có Gọi kim loại là M có Gọi kim loại là M, oxit là A hoá trị n. hoá trị n. hoá trị n gốc axit là B CTHH là: CTHH là: HnB CTHH là: M(OH)n CTHH là: MxBy - A2On nếu n lẻ - AOn/2 nếu n chẵn Gồm 2 loại: Gồm 2 loại: Gồm 2 loại: Gồm 2 loại: + oxit axit: gồm 2 + axit có oxi: H2SO4, + bazơ tan: NaOH, + muối trung hòa: nguyên tố là oxi và HNO3 LiOH, KOH, Ba(OH)2, (không có H) : NaCl, phi kim: P2O5, SO2 + axit không có oxi: Ca(OH)2 CuSO4 + oxit bazơ : gồm 2 HCl + Bazơ không tan: còn +Muối axit: (có H) nguyên tố là oxi và lại Ca(HCO3)2, NaHSO4 kim loại:CuO, Fe2O3 -Tên oxit bazơ = - Axit không có oxi -Tên bazơ = Tên kim Tên muối trung hòa tên nguyên tố( hóa = Axit + tên phi kim loại + hidroxit = tên kim loại ( Kèm trị nếu kim loại + hidric Lưu ý: Kèm theo hoá trị theo hoá trị của kim nhiều hóa trị) + oxit HCl: axit clohidric của kim loại khi kim loại khi kim loại có K2O: kali oxit - Axit có ít oxi = loại có nhiều hoá trị. nhiều hoá trị)+ tên CuO: đổng (II) oxit Axit + tên phi kim + NaOH: natri hidroxit gốc axit -Tên oxit axit =tiền ơ (rơ) Fe(OH)3:sắt(III)hidroxit Na2SO4: natri sunfat tố chỉ số nguyên tử H2SO3: axit sunfurơ Fe(NO3)2: sắt (II) phi kim + Tên phi HNO2: axit nitrơ nitrat kim+ tiền tố chỉ số - Axit có nhiều oxi Tên muối axit = tên nguyên tử oxi + oxit = Axit + tên phi kim kim loại ( Kèm theo + ic (ric) hoá trị của kim loại 5 Tiền tố: đi: 2; tri : 3: H2SO4: axit sunfuric khi kim loại có nhiều tetra: 4; penta: 5. HNO3: axit nitric hoá trị)+ tiền tố chỉ SO2: lưu huỳnh nguyên tố H+ hidro+ đioxit tên gốc axit P2O5 : điphotpho NaH2PO4: natri pentaoxit đihidrophotphat CaHPO4: canxi hidrophotphat II- BÀI TẬP VẬN DỤNG Câu 1: Phân tử khối của KMnO4 là A. 158. B. 226. C. 256. D. 326. Câu 2: Cho Ca(II), PO4(III), công thức hóa học nào viết đúng? A. CaPO4. B. Ca2PO4. C. Ca3(PO4)2. D. Ca3PO4. Câu 3: Chất nào sau đây là oxit ? A. H2SO4. B. Na2SO3. C. CO2. D. KOH. Câu 4: Chất nào sau đây là axit ? A. NaOH. B. KHCO3. C. Ba(HSO3)2. D. H2CO3. Câu 5: Chất nào sau đây là muối trung hòa ? A. HCl. B. CaCO3. C. NaHSO4. D. Fe(OH)3. Câu 6: Lập các PTHH sau: a) Na + O2 → Na2O b) Fe + HCl → FeCl2 + H2 c) Al2O3 + HCl → AlCl3 + H2O d) NaOH + CuSO4 → Cu(OH)2 + Na2SO4 e) Al2(SO4)3 + BaCl2 → AlCl3 + BaSO4 f) Fe(OH)3 → Fe2O3 + H2O g) CaO + HNO3 → Ca(NO3)2 + H2O Câu 7: Cho 8,4 gam Fe tác dụng vừa đủ với dung dịch HCl, sau phản ứng thu được FeCl2 và khí H2 (đktc) a, Lập PTHH của phản ứng b, Tính khối lượng HCl và khối lượng FeCl2 thu được c, Tính thể tích khí H2 thu được ở đktc Câu 8: Hoàn thành 2 bảng sau: 6 STT Nguyên tố Công thức của oxit Tên gọi Công thức của bazơ Tên bazơ tương ứng tương ứng gọi 1 Na 2 Ca 3 Mg 4 Fe (Hoá trị II) 5 Fe (Hoá trị III) STT Nguyên tố Công thức của oxit Tên gọi Công thức của axit Tên axit tương ứng tương ứng gọi 1 S (Hoá trị VI) 2 P (Hoá trị V) 3 C (Hoá trị IV) 4 S (Hoá trị IV) Câu 9: Gọi tên các muối có CTHH sau: a, Na2CO3 b, BaSO4 c, Fe(NO3)3 d, KHSO3 Câu 10: Viết CTHH của các hợp chất ứng với tên gọi sau đây: a) Bari oxit b) Kali nitrat c) Canxi clorua d) Đồng(II) hidroxit e) Natri Sunfit f) Bạc oxit 7 III-ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI Câu 1 : Chọn A Câu 2: Chọn C Câu 3: Chọn C Câu 4: Chọn D Câu 5: Chọn B Câu 6: a) 4Na + O2 → 2Na2O b) Fe + 2HCl → FeCl2 + H2 c) Al2O3 + 6HCl → 2AlCl3 + 3H2O d)2NaOH + CuSO4 → Cu(OH)2 + Na2SO4 e)Al2(SO4)3 + 3BaCl2 → 2AlCl3 + 3BaSO4 f)2Fe(OH)3 → Fe2O3 + 3H2O g)CaO + 2HNO3 → Ca(NO3)2 + H2O Câu 7: cách làm tương tự ví dụ 2 (HS làm và đối chiếu với đáp án) a, Fe + 2HCl → FeCl2 + H2 b, mHCl = 10,95g ; mFeCl2 = 19,05 g c, VH2 = 3,36 lít Câu 8: STT Nguyên tố Công thức Tên gọi Công thức của bazơ Tên gọi của oxit bazơ tương ứng 1 Na Na2O Natri oxit NaOH Natri hidroxit 2 Ca CaO Canxi oxit Ca(OH)2 Canxi hidroxit 3 Mg MgO Magie oxit Mg(OH)2 Magie hidroxit 4 Fe (Hoá trị II) FeO Sắt(II) oxit Fe(OH)2 Sắt(II) hidroxit 8 5 Fe (Hoá trị Fe2O3 Sắt(III) oxit Fe(OH)3 Sắt(III) III) hidroxit STT Nguyên tố Công thức Tên gọi Công thức của axit Tên gọi của oxit axit tương ứng 1 S (Hoá trị VI) SO3 Lưu huỳnh H2SO4 Axit sunfuric trioxit 2 P (Hoá trị V) P2O5 Điphotpho H3PO4 Axit pentaoxit photphoric 3 C (Hoá trị IV) CO2 Cacbon H2CO3 Axit cacbonic đioxit 4 S (Hoá trị IV) SO2 Lưu huỳnh H2SO3 Axit sunfurơ đioxit Câu 9: a, natri cacbonat b, bari sunfat c, sắt (III) nitrat d, kali hidrosunfit Câu 10: a) Bari oxit: BaO b) Kali nitrat: KNO3 c) Canxi clorua: CaCl2 d) Đồng(II) hidroxit: Cu(OH)2 e) Natri Sunfit: Na2SO3 f) Bạc oxit: Ag2O 9
File đính kèm:
 noi_dung_on_tap_mon_hoa_hoc_9_chu_de_1_on_tap_dau_nam.docx
noi_dung_on_tap_mon_hoa_hoc_9_chu_de_1_on_tap_dau_nam.docx

