Nội dung Ôn tập môn Hóa Học 9 - Chủ đề 2: Oxit
I-KIẾN THỨC TRỌNG TÂM CẦN NẮM
1. TÍNH CHẤT HÓA HỌC CỦA OXIT
2. KHÁI QUÁT VỀ SỰ PHÂN LOẠI OXIT
-Oxit bazơ là những oxit tác dụng với dung dịch axit tạo muối và nước
-Oxit axit là những oxit tác dụng với dung dịch bazo tạo muối và nước
-Oxit lưỡng tính là những oxit vừa tác dụng được với dung dịch bazo, vừa tác dụng được với dung dịch axit. VD như Al2O3, ZnO...
-Oxit trung tính là những oxit không tác dụng với axit, bazo, nước. VD như CO, NO, SO....
II-BÀI TẬP MẪU CÓ HƯỚNG DẪN
*Dạng bài tập viết PTHH dựa vào tính chất hóa học
Bài 1: Có những oxit sau: Fe2O3, CaO, K2O, CuO, SO2, SO3, CO, P2O5. Những oxit nào tác dụng với:
a) H2O b)dd H2SO4 c) dd NaOH
Viết các PTHH của các phản ứng xảy ra?
Bài 2: Bằng phương pháp hoá học, hãy nhận biết 2 chất khí đựng trong 2 bình riêng biệt sau: CO, CO2
Bài 3: Bằng phương pháp hoá học hãy nhận biết các chất rắn riêng biệt sau:
Na2O, MgO và P2O5
Bài 4: Hòa tan 6,2 gam Na2O vào nước thu được 2 lít dung dịch bazơ .
a) Tính khối lượng bazơ thu được
b) Tính nồng độ mol của dung dịch bazơ thu được
Bài 5: Hòa tan 16 gam SO3 trong nước thu được 250 ml dung dịch axit.
a) Tính khối lượng axit thu được
b) Nồng độ mol dung dịch axit thu được là bao nhiêu ?
Tóm tắt nội dung tài liệu: Nội dung Ôn tập môn Hóa Học 9 - Chủ đề 2: Oxit
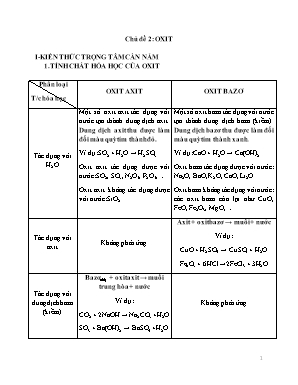
Chủ đề 2: OXIT I-KIẾN THỨC TRỌNG TÂM CẦN NẮM 1. TÍNH CHẤT HÓA HỌC CỦA OXIT Phân loại OXIT AXIT OXIT BAZƠ T/c hóa học Một số oxit axit tác dụng với Một số oxit bazơ tác dụng với nước nước tạo thành dung dịch axit. tạo thành dung dịch bazơ (kiềm). Dung dịch axit thu được làm Dung dịch bazơ thu được làm đổi đổi màu quỳ tím thành đỏ. màu quỳ tím thành xanh. Tác dụng với Ví dụ: SO2 + H2O → H2SO3 Ví dụ: CaO + H2O → Ca(OH)2 H2O Oxit axit tác dụng được với Oxit bazơ tác dụng được với nước: nước: SO2, SO3, N2O5, P2O5, Na2O, BaO, K2O, CaO, Li2O Oxit axit không tác dụng được Oxit bazơ không tác dụng với nước: với nước: SiO2 các oxit bazo còn lại như CuO, FeO, Fe2O3, MgO, Axit + oxit bazơ → muối + nước Tác dụng với Ví dụ: Không phản ứng axit CuO + H2SO4 → CuSO4 + H2O Fe2O3 + 6HCl →2FeCl3 + 3H2O Bazơ(dd) + oxit axit → muối trung hòa + nước Tác dụng với dung dịch bazơ Ví dụ: Không phản ứng (kiềm) CO2 + 2NaOH → Na2CO3 +H2O SO3 + Ba(OH)2 → BaSO4 +H2O 1 Tác dụng với Oxit axit + oxit bazơ → muối Không phản ứng oxit axit Ví dụ: CaO + CO2 → CaCO3 Tác dụng với Oxit bazơ + oxit axit → muối Không phản ứng oxit bazơ Ví dụ: CaO + SO3 → CaSO4 2. KHÁI QUÁT VỀ SỰ PHÂN LOẠI OXIT -Oxit bazơ là những oxit tác dụng với dung dịch axit tạo muối và nước -Oxit axit là những oxit tác dụng với dung dịch bazo tạo muối và nước -Oxit lưỡng tính là những oxit vừa tác dụng được với dung dịch bazo, vừa tác dụng được với dung dịch axit. VD như Al2O3, ZnO... -Oxit trung tính là những oxit không tác dụng với axit, bazo, nước. VD như CO, NO, SO.... II-BÀI TẬP MẪU CÓ HƯỚNG DẪN *Dạng bài tập viết PTHH dựa vào tính chất hóa học Bài 1: Có những oxit sau: Fe 2O3, CaO, K2O, CuO, SO2, SO3, CO, P2O5. Những oxit nào tác dụng với: a) H2O b)dd H2SO4 c) dd NaOH Viết các PTHH của các phản ứng xảy ra? Hướng dẫn: a) Những oxit tác dụng với nước gồm: CaO, K2O, SO2, SO3, P2O5 CaO + H2O → Ca(OH)2 K2O + H2O → 2KOH SO2 + H2O → H2SO3 2 SO3 + H2O → H2SO4 P2O5 + 3H2O → 2H3PO4 b) Những oxit tác dụng với dd H2SO4 là: CaO, Fe2O3, K2O, CuO CaO + H2SO4 → CaSO4 + H2O Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O K2O + H2SO4 → K2SO4 + H2O CuO + H2SO4 → CuSO4 + H2O c) Những oxit tác dụng với dd NaOH là SO2, SO3, P2O5 SO2 + 2NaOH → Na2SO3 + H2O SO3 + 2NaOH → Na2SO4 + H2O P2O5 + 6NaOH → 2Na3PO4 + 3H2O Vì CO là oxit trung tính nên không tác dụng với nước, axit, bazo *Dạng bài tập nhận biết chất bằng phương pháp hóa học Bài 2: Bằng phương pháp hoá học, hãy nhận biết 2 chất khí đựng trong 2 bình riêng biệt sau: CO, CO2 Hướng dẫn: Dẫn 2 khí qua dung dịch nước vôi trong Ca(OH)2 → nhận biết CO2 làm đục nước vôi trong, CO không phản ứng. CO2 + Ca(OH)2 → CaCO3↓ + H2O Để nhận biết CO2 ta dùng dung dịch Ca(OH)2 và ngược lại Bài 3: Bằng phương pháp hoá học hãy nhận biết các chất rắn riêng biệt sau: Na2O, MgO và P2O5 Hướng dẫn: 3 Cách 1: - Hoà tan 3 mẫu thử vào nước, nhận biết được MgO không tan; hai mẫu thử còn lại tan tạo dung dịch trong suốt. - Thử giấy quì tím với hai dung dịch vừa tạo thành, nếu giấy quì tím chuyển sang đỏ là dung dịch axit => chất ban đầu là P 2O5; nếu quì tím chuyển sang xanh là dung dịch bazơ => chất ban đầu là Na2O. PTHH: Na2O + H2O → 2NaOH P2O5 + 3H2O → 2H3PO4 Cách 2: Thay vì dùng nước và quỳ tím để nhận biết, ta chỉ cần dùng quỳ tím ẩm - Nhúng quỳ tím ẩm lần lượt vào 3 mẫu thử trên, nếu giấy quì tím ẩm chuyển sang đỏ là mẫu thử P2O5; nếu quì tím ẩm chuyển sang xanh là mẫu thử Na2O, nếu không có hiện tượng là mẫu thử MgO *Dạng bài tập tính toán theo PTHH Bài 4: Hòa tan 6,2 gam Na2O vào nước thu được 2 lít dung dịch bazơ . a) Tính khối lượng bazơ thu được b) Tính nồng độ mol của dung dịch bazơ thu được Hướng dẫn: -Tính số mol Na2O: 6,2 = = = 0,1 mol 푛 2O 62 -Viết PTHH, tính số mol các chất theo PTHH Na2O + H2O → 2NaOH 1 mol 1 mol 2 mol 0,1 mol → 0,1 mol → 0,2 mol -Tính theo yêu cầu của đề bài a) Khối lượng bazo thu được là: mNaOH = n.M = 0,2 . 40 = 8 gam b) –Công thức tính nồng độ mol (CM) là 풏 C = trong đó n là số mol M 푽풅풅 Vdd là thể tích dung dịch ( đơn vị lít) -Nồng độ mol của dung dịch NaOH thu được là: 푛 0,2 CM = = = 0,1 (M) 2 4 Bài 5: Hòa tan 16 gam SO3 trong nước thu được 250 ml dung dịch axit. a) Tính khối lượng axit thu được b) Nồng độ mol dung dịch axit thu được là bao nhiêu ? Hướng dẫn: Cách làm tương tự bài 4 (HS làm thử và đối chiếu với đáp án) a, m = 19,6 gam b, CM = 0,8 (M) III- BÀI TẬP VẬN DỤNG Câu 1: Oxit nào sau đây là oxit bazơ? A. P2O5. B. SO2. C. CaO. D. CO. Câu 2: Oxit nào sau đây là oxit axit? A. SO2. B. Na2O. C. Al2O3. D. CO. Câu 3: Oxit nào sau đây là oxit lưỡng tính? A. BaO. B. Al2O3. C. SO3. D. MgO. Câu 4: Oxit nào sau đây là oxit trung tính? A. CaO. B. CO2. C. SO2. D. CO. Câu 5: Chất tác dụng với nước tạo ra dung dịch bazơ là A. K2O. B. CuO. C. CO. D. SO2. Câu 6: Chất tác dụng với nước tạo ra dung dịch axit là A. Ag2O. B. CuO. C. P2O5. D. CaO. Câu 7: Dãy oxit tác dụng được với dung dịch NaOH là: A. CuO, Fe2O3, SO2, CO2. B. CaO, CuO, CO, N2O5. C. CO2, SO2, P2O5, SO3. D. SO2, MgO, CuO, Ag2O. Câu 8: Để loại bỏ khí CO2 có lẫn trong hỗn hợp (O2, CO2), người ta cho hỗn hợp đi qua dung dịch chứa: A. HCl. B. Ca(OH)2. C. Na2SO4. D. NaCl. Câu 9: Oxit tác dụng với nước tạo ra dung dịch làm quỳ tím hóa xanh là A. CaO. B. P2O5. C. Fe2O3. D. MgO. Câu 10: Để nhận biết 2 lọ mất nhãn đựng CaO và MgO ta dùng: A. HCl. B. NaOH. C. HNO3. D. Quỳ tím ẩm. Câu 11: Dãy các oxit tác dụng được với dung dịch HCl là A. CO, CaO, CuO, FeO. B. NO, Na2O, CuO, Fe2O3. C. SO2, CaO, CuO, FeO. D. CuO, CaO, Na2O, FeO. Câu 12: Sau khi đốt photpho trong bình có một ít nước. Lắc bình một lúc, dung dịch trong bình : A. làm quì tím chuyển sang màu đỏ. B. làm quì tím chuyển sang màu xanh. 5 C. làm quì tím mất màu. D. không làm thay đổi màu quì tím. Câu 13: Hoà tan 23,5 gam kali oxit vào nước được 0,5 lít dung dịch bazo. Nồng độ mol của dung dịch bazo thu được là : A. 0,25M. B. 0,5M. C. 1M. D. 2M. Câu 14: Cho 50 gam khí SO3 hợp nước tạo ra axit H2SO4. Khối lượng axit thu được là : A. 14,7 gam. B. 22,05 gam. C. 25,05 gam. D. 61,25 gam. Câu 15: Cho 32 gam CuO phản ứng vừa đủ với 800 ml dung dịch HCl. Khối lượng muối tạo thành và nồng độ mol của dung dịch HCl tương ứng là: A. 54 gam; 2 M. B. 27 gam; 1 M. C. 54 gam; 1 M. D. 27 gam; 2M. Đáp án: Câu 1 2 3 4 5 6 7 8 9 Đáp C A B D A C C B A án Câu 10 11 12 13 14 15 Đáp án D D A C D C * Hướng dẫn câu 13,14,15 -Cách làm tương tự như bài tập mẫu -Sử dụng các công thức tính toán: .Tính số mol: n = . Tính khối lượng: m = n.M 풏 . Tính nồng độ mol: C = M 푽풅풅 6
File đính kèm:
 noi_dung_on_tap_mon_hoa_hoc_9_chu_de_2_oxit.docx
noi_dung_on_tap_mon_hoa_hoc_9_chu_de_2_oxit.docx

