Giáo án Hóa học 9 - Tuần 5 - Năm học 2023-2024 - Lê Thị Hoàn
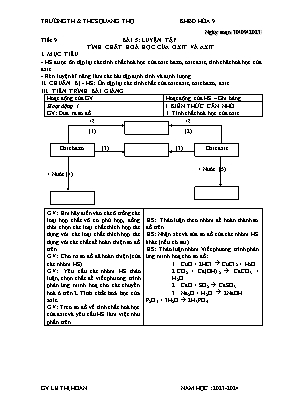
GV: Em hãy điền vào các ô trống các loại hợp chất vô cơ phù hợp, đồng thời chọn các loại chất thích hợp tác dụng với các loại chất thích hợp tác dụng với các chất để hoàn thiện sơ đồ trên
GV: Cho nx sơ đồ đã hoàn thiện (của các nhóm HS)
GV: Yêu cầu các nhóm HS thảo luận, chọn chất để viết phương trình phản ứng minh hoạ cho các chuyển hoá ở trên 2. Tính chất hoá học của axit.
GV: Treo sơ đồ về tính chất hoá học của axit và yêu cầu HS làm việc như phần trên.
Bạn đang xem tài liệu "Giáo án Hóa học 9 - Tuần 5 - Năm học 2023-2024 - Lê Thị Hoàn", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Giáo án Hóa học 9 - Tuần 5 - Năm học 2023-2024 - Lê Thị Hoàn
TRƯỜNG TH & THCS QUANG THỌ KHBD HÓA 9 Ngày soạn 30/09/2023 Tiết 9 BÀI 5: LUYỆN TẬP TÍNH CHẤT HOÁ HỌC CỦA OXIT VÀ AXIT I. MỤC TIÊU - HS được ôn tập lại các tính chất hoá học của oxit bazơ, oxit axit, tính chât hoá học của axit - Rèn luyện kĩ năng làm các bài tập định tính và định lượng II. CHUẨN BỊ - HS: Ôn tập lại các tính chất của oxit axit, oxit bazơ, axit III. TIẾN TRÌNH BÀI GIẢNG Hoạt động của GV Hoạt động của HS – Ghi bảng Hoạt động 1 I. KIẾN THỨC CẦN NHỚ GV: Đưa ra sơ đồ 1. Tính chất hoá học của oxit +? +? (1) (2) Oxit bazơ (3) (3) Oxit axit + Nước (5) + Nước (4) GV: Em hãy điền vào các ô trống các loại hợp chất vô cơ phù hợp, đồng HS: Thảo luận theo nhóm để hoàn thành sơ thời chọn các loại chất thích hợp tác đồ trên. dụng với các loại chất thích hợp tác HS: Nhận xét và sửa sơ đồ của các nhóm HS dụng với các chất để hoàn thiện sơ đồ khác (nếu có sai) trên HS: Thảo luận nhóm.Viết phương trình phản GV: Cho nx sơ đồ đã hoàn thiện (của ứng minh hoạ cho sơ đồ: các nhóm HS) 1. CuO + 2HCl CuCl2 + H2O GV: Yêu cầu các nhóm HS thảo 2.CO2 + Ca(OH)2 CaCO 3 + luận, chọn chất để viết phương trình H2O phản ứng minh hoạ cho các chuyển 2. CaO + SO2 CaSO3 hoá ở trên 2. Tính chất hoá học của 3. Na2O + H2O 2NaOH axit. P2O5 + 3H2O 2H3PO4 GV: Treo sơ đồ về tính chất hoá học của axit và yêu cầu HS làm việc như phần trên. GV LÊ THỊ HOÀN NĂM HỌC : 2023-2024 TRƯỜNG TH & THCS QUANG THỌ KHBD HÓA 9 + D + Quì tím A + B (1) Màu đỏ (4) axit A + C + E + G A + C (2) (3) Yêu cầu HS: Viết phương trình phản ứng minh hoạ HS: Viết phương trình phản ứng: cho các chất của axit (thể hiện ở sơ đồ 1. 2HCl + Zn ZnCl2 + H2 trên). 2. 3H2SO4 + Fe2O3 Fe2(SO4)3 + 3H2O Tổng kết lại: Em hãy nhắc loại các tính 3. H2SO4 + Fe(OH)2 FeSO4 + 2H2O chất hoá học của oxit axit, oxit bazơ, HS: Nhắc lại các tính chất hoá học của oxit axit. axit, oxit bazơ, axit Hoạt động 2 Bài tập Bài tập 1: Cho các chất sau: HS: Làm bài tập 1. SO2, CuO, Na2O, CaO, CO2 a)Những chất tác dụng được với nước là : Hãy cho biết những chất nào tác dụng SO2, Na2O, CO2, CaO đợc với: b)Những chất tác dụng được với axit HCl là a. Nước; : CuO, Na2O, CaO b. Axit clohiđric c)Những chất tác dụng được với dung dịch c. Natri hiđroxit NaOH là: SO2, CO2. Viết phương trình phản ứng (nếu có) HS: Làm bài tập 2: => Gợi ý HS làm bài (nếu cần): a. Phương trình phản ứng Nêu bài luyện tập 2: Mg + 2HCl MgCl2 + H2 Bài tập 2: Hoà tan 1,2 gam Mg bằng nHClbanđâu= CM x V = 3 x 0,05 = 0,15 50ml dung dịch HCl 3M. (mol) a. Viết phơng trình phản ứng. 1,2 b. Tính thể tích khí thoát ra (ở đktc). b. nMg= = 0,05 (mol) c. Tính nồng độ mol của dung dịch 24 thu được sau phản ứng (coi thể tích theo phương trình : cảu dung dịch sau phản ứng thay đổi nH2= nMgCl2 = nMg = 0,05 (mol) không đáng kể so với thể tích của nHCl = 2 x nMg= 2 x 0,05 = 0,1 (mol) dung dịch HCl đã dùng). VH2= n x 22,4 = 0,05 x 22,4 = 1,12 (lít). => Gọi một HS nhắc lại các bước của c. Dung dịch sau phản ứng có MgCl 2 HCl 0,05 bài tập tính theo phơng trình. dư n 0,05 Gọi HS nhắc lại các công thức phải sử 0,05 V 0,05 dụng trong bài CM MgCl2 = = = 1M Yêu cầu HS làm bài tập 2 vào vở nHCl dư= nHCl ban đầu – nHCl phản ứng= 0,15 – 0,1 Gv chữa bài lên bảng = 0,05 mol + axit + Bazơ (2) Muối n (1) CM HCl (d) = = 1M V Oxit bazơ (3) Muối (3) Oxit axit GV LÊ THỊ HOÀN NĂM HỌC : 2023-2024 + Nước (5) + Nước (4) dd axit DD bazơ TRƯỜNG TH & THCS QUANG THỌ KHBD HÓA 9 4) Củng cố - Đánh giá- Củng cố lại kiến thức lí thuyết HS cần nhớ - Nhắc nhở HS một số sai sót thường gặp khi làm bài tập hoá học 5) Hướng dẫn về nhà: - Làm bài tập:2, 4 SGK - 5.1, 5.2, 5.3, 5.4, 5.5, 5.6, 5.7 SBT - Chuẩn bị thực hành: kẻ tường trình, CaO, diêm, đóm, chậu nước, khăn lau sạch. BT 2: a) Cả 5 oxit đã cho b) Những oxit là: CuO, CO2 điều chế bằng phân huỷ Tiết 10 BÀI 6: THỰC HÀNH TÍNH CHẤT HÓA HỌC CỦA OXIT VÀ AXIT A- MỤC TIÊU: 1. Kiến thức:- Khắc sâu kiến thức về tính chất hoá học của oxit, axit. 2. Kĩ năng:- Biết cách sử dụng dụng cụ thí nghiệm, cách hoà tan một chất - Biêta cách quan sát hiện tượng, ghi chép và rút ra kết luận - Tiếp tục rèn luyện kĩ năng về thực hành hoá học, giải bài tập thực hành hoá học; Kĩ năng làm thí nghiệm hoá học với lượng nhỏ hoá chất - Giáo dục cho HS ý thức tiết kiệm, cẩn thận... trong học tập và trong thực hành hoá học. Biết giữ vệ sinh sạch sẽ phòng thí nghiệm, lớp học B - CHUẨN BỊ - Dụng cụ: -Hoá chất: - Giá ống nghiệm : 1 chiếc - Canxi oxit; P đỏ - ống nghiệm : 10 chiếc - Dungdịch HCl;Na2SO4; - Kẹp gỗ : 1 chiếc NaCl; BaCl2 ; H2O - Lọ thuỷ tinh miệng rộng:1 chiếc - Quì tím - Muôi sắt : 1 chiếc C - TIẾN TRÌNH DẠY HỌC: 1- Ổn định tổ chức: 2- Kiểm tra: Kiểm tra sự chuẩn bị của HS ( Bản tường trình, hoá chất... ) 3- Bài mới : Hoạt động của GV Hoạt động của HS – Ghi bảng Hoạt động 1 Kiểm tra phần lý thuyết có liên quan đến nội dung bài thực hành HS: Kiểm tra bộ dụng cụ, hoá chất GV: Kiểm tra sự chuẩn bị của phòng thí nghiệm thực hành của nhóm mình. (dụng cụ, hoá chất cho buổi thực hành). Hoạt động 2 tiến hành thí nghiệm a, thí nghiệm 1: Phản ứng của canxi với nước 1. Tính chất hoá học của oxit GV: Hướng dẫn HS làm bài thí nghiệm 1: HS: Làm thí nghiệm - Cho 1 mẩu CaO vào ống nghiệm, sau đó thêm HS: Nhận xét hiện tượng: dần 1 2 ml H2O quan sát hiện tượng xẩy ra. - Mẫu CaO nhão ra. GV: - Thử dung dịch sau phản ứng bằng giấy qùi - Phản ứng toả nhều nhiệt tím hoặc dung dịch phenolphtalein màu của thuốc - Thử dung dịch sau phản ứng thủ thay đổi thế nào? Vì sao? bằng giấy quì tím : giấy quì tím Kết luận về tính chất hoá học của CaO và viết ph- bị chuyển sang màu xanh ( ương trình phản ứng minh hoạ dung dịch thu được có tính b. Thí nghiệm 2: Phản ứng của điphotpho bazơ) pentaoxit với nớc. PTHH: CaO + H2O Ca(OH)2 GV LÊ THỊ HOÀN NĂM HỌC : 2023-2024 TRƯỜNG TH & THCS QUANG THỌ KHBD HÓA 9 GV: Hướng dẫn HS làm thí nghiệm và nêu các HS: yêu cầu đối với HS. + Làm thí nghiệm + Đối một ít photpho đỏ (bằng hạt đậu xanh) + Nhận xét hiện tượng: trong bình thuỷ tinh miệng rộng. Sau khi P đỏ Phốt pho đỏ trong bình tạo thành chảy hết, cho 3ml H2O vào bình, đậy nút, lắc nhẹ những hạt nhỏ màu trắng, tan được quan sát hiện tượng? trong nước tạo thành dung dịch trong + Thử dung dịch thu được bằng quì tím, các em suốt. hãy nhận xét sự đổi màu của quì tím. - Nhúng một mẩu quì tím vào + Kết luận về tính chất hoá học của điphotpho dung dịch đó, quì tím hoá đỏ, pentaoxit. Viết các phương trình hoá học. chứng tỏ dung dịch thu được có 2. Nhận biết các dung dịch. tính axit thí nghiệm 3: Có 3 lọ không nhãn, mỗi lọ đựng Kết luận: Điphôtpho pentaoxit(P2O5) một trong ba dung dịch là : H2SO4, HCl, Na2SO4. có tính chất của oxitaxit Hãy tiến hành những thí nghiệm nhận biết các lọ 0 t , hoá chất đó. 4P + 5O2 2P2O5 GV: Hướng dẫn HS cách làm: + Để phân biệt được các dung dịch trên, ta phải P2O5 + 3H2O 2H3PO4 biết sự khác nhau về tính chất của các dung dịch HS: Phân loại và gọi tên đó (GV gọi một HS phân loại và gọi tên 3 chất). HCl : Axit clohiđric (axit) + Ta dựa vào tính chất khác nhau của các loại hợp H2SO4: Axit sunfuric (axit) chất đó để phân biệt chúng : đó là t/c nào Na2SO4 : natri sunfat (muối) HS: Tính chất khác nhau giúp ta phân GV: Gọi một HS nêu cách làm. biệt được các hợp chất đó là: - Dung dịch axit làm cho quì tím hoá đỏ. GV: Yêu cầu các nhóm tiến hành làm thí nghiệm - Nếu nhỏ dung dịch BaCl2 vào 2 dung 3 (sau khi đó chốt lại cách làm). dịch HCl và H2SO4 thì chỉ có dung Yêu cầu các nhóm báo cáo kết quả theo mẫu. dịch H2SO4 xuất hiện kết tủa trắng. HS: Làm thí nghiệm 3. HS: Nêu cách làm : HS: Đại diện các nhóm báo cáo kết quả thực + Ghi số thứ tự 1, 2, 3 cho mỗi lọ đựng hành dung dịch ban đầu. Lọ 1 đựng dung dịch.......... Bước 1: Lấy ở mỗi lọ một giọt nhỏ vào Lọ 2 đựng dung dịch ......... mẩu giấy quì tím. Lọ 3 đựng dung dịch .......... -Nếu quì tím không đổi màu thì lọ số ...... đựng dung dịch Na2SO4 -Nếu quì tím đổi sang đỏ, lọ số...... và lọ số .....đọng dung dịch axit Bước 2: Lấy ở mỗi lọ chứa dung dịch Hoạt động 3. Viết bản tường trình axit 1ml dung dịch cho vào ống nghiệm, nhỏ một giọt dung dịch BaCl2 vào mỗi ống nghiệm. -Nếu trong ống nghiệm nào xuất hiện kết tủa trắng thì lọ dung dịch ban đầu có số ......... Là dung dịch H2SO4. -Nếu không có kết tủa thì lọ ban đầu có số....... là dung dịch HCl. H2SO4(dd) + BaCl2(dd) BaSO 4(r) + 2HCl(dd) GV LÊ THỊ HOÀN NĂM HỌC : 2023-2024 TRƯỜNG TH & THCS QUANG THỌ KHBD HÓA 9 III) tường trình HS hoàn thiện tường trình 4)Củng cố - Đánh giá: GV: Nhận xét về ý thức, thái độ của HS trong buổi thực hành. Đồng thời nhận xét về kết quả thực hành của các nhóm. ? Qua giờ TH đã khắc sâu được những kiến thức gì GV: Hướng dẫn HS thu hồi hoá chất, rửa ống nghiệm vệ sinh phòng thực hành. GV LÊ THỊ HOÀN NĂM HỌC : 2023-2024
File đính kèm:
 giao_an_hoa_hoc_9_tuan_5_nam_hoc_2023_2024_le_thi_hoan.docx
giao_an_hoa_hoc_9_tuan_5_nam_hoc_2023_2024_le_thi_hoan.docx

